1 药品临床综合评价项目真实世界研究质量控制规范制定过程和方法
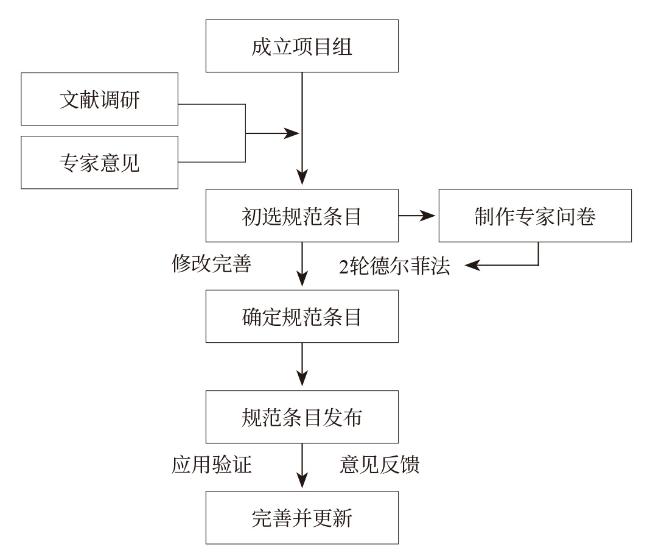
1.1 质量控制规范形成流程
1.2 质量控制规范制定方法
1.2.1 初步遴选质量控制规范条目
1.2.2 起草质量控制规范条目
表1 参与德尔菲法咨询的专家基本信息 |
| 职业 | 第一轮(n = 34) | 第二轮(n = 49) | ||
|---|---|---|---|---|
| 人数/人 | 占比/ % | 人数/人 | 占比/ % | |
| 高校研究者 | 5 | 14.7 | 7 | 14.3 |
| 药师 | 7 | 20.5 | 11 | 22.4 |
| 医生 | 12 | 35.3 | 18 | 36.7 |
| 政府工作人员 | 4 | 11.8 | 1 | 2.1 |
| 医药企业工作人员 | 2 | 5.9 | 7 | 14.3 |
| 其他 | 4 | 11.8 | 5 | 10.2 |
1.2.3 质量控制规范推广和更新
2 药品临床综合评价项目真实世界研究质量控制规范基本特征
2.1 质量控制规范基本特点
2.2 质量控制规范基本内容和结构
3 药品临床综合评价项目真实世界研究质量控制规范条目解读
3.1 研究目的设定(领域1)
3.1.1 研究问题的可操作性(条目1)
3.1.2 研究目的的明确性(条目2)
3.1.3 研究假设的逻辑性(条目3)
3.2 研究设计(领域2)
3.2.1 研究源人群选择的合理性(条目4)
3.2.2 纳入、排除标准的合理性(条目5)
3.2.3 暴露(含对照药物)、结局定义及实操化的合理性(条目6)
3.2.4 协变量及解决潜在偏倚策略的合理性(条目7)
3.2.5 索引日期的定义及分配的合理性(条目8)
3.2.6 样本量计算和预期运行特性(条目9)
3.2.7 随访时间(条目10)
3.3 数据源及预处理(领域3)
3.3.1 数据源描述(条目11)
3.3.2 数据源与研究问题的契合度(条目12)
3.3.3 数据与研究结局的相关性(条目13)
3.3.4 数据采集过程的规范性(条目14)
3.3.5 数据清洗过程的合理性(条目15)
3.3.6 数据验证(条目16)
3.3.7 数据管理计划(条目17)
3.3.8 医学伦理审查中的知情同意与隐私保护(条目18)
3.4 统计分析(领域4)
3.4.1 使用统计分析计划(条目19)
3.4.2 评估治疗效果的分析方法的合理性(条目20)
3.4.3 控制潜在混杂因素的分析方法(条目21)
3.4.4 因果路径中间变量过度调整评估(条目22)
3.4.5 亚组分析方法(条目23)
3.4.6 控制组间差异的方法(条目24)
3.4.7 控制逆向因果的方法(条目25)
3.4.8 缺失值及分类错误数据的处理方法(条目26)
3.4.9 处理多重性的方法(条目27)
3.4.10 敏感性分析(条目28)
3.5 结果及解读(领域5)
3.5.1 报告完整性(条目29)
3.5.2 研究对象基本资料(条目30)
3.5.3 描述性结果或主要结果及结局资料(条目31)
3.5.4 结果解读及局限性阐述(条目32)
3.5.5 结果外推性(条目33)
3.5.6 成果转化(条目34)
3.5.7 潜在利益冲突(条目35)
3.5.8 方案、数据、编码可获得性(条目36)
4 药品临床综合评价项目真实世界研究质量控制规范应用
表2 不同类型真实世界研究质量控制指标条目适用性区分 |
| 条目 | 前瞻性研究 | 回顾性研究 | |||
|---|---|---|---|---|---|
| 随机或非随机临床试验 | 疾病登记库 | 队列研究 | 病例对照研究 | 横截面研究 | |
| 研究目的设定(领域1) | 1~3 | 1~3 | 1~3 | 1~3 | 1~3 |
| 研究设计(领域2) | 4~10 | 4~8,10 | 4~10 | 4~9 | 4~8 |
| 数据源及预处理(领域3) | 14~18 | 14~18 | 11~18 | 11~18 | 11~18 |
| 统计分析(领域4) | 19~28 | 19~28 | 19~28 | 19~28 | 19~28 |
| 结果及解读(领域5) | 29~36 | 29~36 | 29~36 | 29~36 | 29~36 |
| 合计 | 1~10,14~36 | 1~8,10,14~36 | 1~36 | 1~9,11~36 | 1~8,11~36 |
5 小结
附录A 药品临床综合评价项目真实世界研究质量控制规范术语解释表
表A.1 药品临床综合评价项目真实世界研究质量控制规范术语解释表 |
| 术语 | 描述 | 案例解释 |
|---|---|---|
| 选择偏倚 | 指在研究设计或实施过程中,由于样本的选择方式不当,导致研究结果不能正确反映总体真实情况的系统性误差 | 如研究1种新药在治疗高血压患者中的效果。选择了1组在大型城市医院就诊的高血压患者作为研究对象。然而,这可能会产生选择偏倚,因为这些患者可能与总体高血压患者不同。比如,城市医院的患者可能比农村地区的患者具有更高的经济水平,或者有更好的医疗可及性,这可能影响他们对治疗的依从性以及健康结果 |
| 左截断 | 指研究对象只在某个事件(如诊断、治疗开始等)发生后才进入研究,而未能观察到事件之前情况 | 研究癌症患者的生存时间,并以确诊日作为研究的起点。如果只纳入确诊后依然存活的患者,就可能会遗漏那些已经在确诊时或确诊前死亡的患者,这就是左截断,那些存活时间短的患者根本没有机会被包括在研究中 |
| 左删失 | 指无法确定某个事件在观察期之前具体发生的时间,但知道该事件在某个时间点之前已经发生了 | 在对糖尿病患者的研究中,研究者记录了患者的首次胰岛素使用时间。如果在观察期内遇到某些已经在使用胰岛素的患者,但不知道他们开始使用胰岛素的确切时间,这就是左删失 |
| 索引日期 | 指在研究中,为每个研究对象设定的特定时间点,用作分析的起点 | 假设进行1项关于他汀类药物与心血管事件风险的研究。索引日期可以设定为患者首次服用他汀类药物的日期。从该日期开始,研究者可以跟踪患者是否在接下来的几年中出现心血管事件,并评估他汀类药物的预防效果 |
| 永生时间偏倚 | 指在观察性研究中,由于暴露定义或随访期间的时间不当分配,导致一些研究对象在某段时间内“免于”发生研究事件(如死亡、疾病恶化等),从而扭曲研究结果 | 比较使用某种药物与未使用药物的患者之间的死亡率差异。定义“药物暴露组”为那些在随访期内曾经至少连续使用6个月该药物的患者。在实际情况中,如果患者在服用该药物前的几个月就死亡,这些死亡患者就不会被归为药物暴露组,而是留在未暴露组中。暴露组中的患者在药物使用的前6个月是“永生”的,因为在这6个月内没有死亡的患者才能被归类为暴露组。暴露组的死亡率可能会被低估,这就导致了永生时间偏倚,使药物看起来比它实际的效果更好 |
| 中间事件 | 指在研究期间发生的某些事件,介于暴露与结局间,可能会影响结局或暴露与结局关系 | 在1项关于抗癌药物疗效的研究中,患者在接受抗癌药物治疗期间可能会经历肿瘤手术或放疗,这些中间事件可能会改变药物对患者结局(如生存时间)的影响 |
| 延迟分析 | 用于评估某一变量(如政策、事件或干预)对另一变量(如经济指标或健康结果)影响的时间延迟 | 在研究某种公共卫生干预措施对感染率的影响时,通常会进行延迟分析,评估接种后的1个月、2个月和3个月的感染率变化。通过建立回归模型,将接种人数的滞后值作为自变量,分析其对当前感染率的影响,从而识别接种效果的时间延迟。这将帮助公共卫生决策者了解何时最有效地实施干预措施 |
| 倾向评分匹配 | 用于评估干预或治疗效果。通过匹配具有相似倾向评分的个体,使得干预组和对照组在观察到的特征上尽可能相似,从而更准确地估计干预的影响 | 研究1种新药对高血压患者的影响,患者分为接受新药治疗组和未接受新药治疗组。使用逻辑回归模型计算每位患者接受新药的倾向评分,然后根据倾向评分进行匹配,以确保2个组在年龄、性别、病史等重要特征上尽量相似。在匹配后的样本中比较2组患者的血压变化,从而更准确地评估新药的治疗效果 |
| Ⅰ类错误 | 为统计假设检验中的概念,指在零假设成立的情况下,错误地拒绝了零假设的错误 | 评估新药对疾病的治疗效果,设定零假设为“新药没有效果”。经过统计分析,研究者得出结论,拒绝了零假设,认为新药有效。如果实际情况是新药确实没有效果,那么就犯了Ⅰ类错误 |